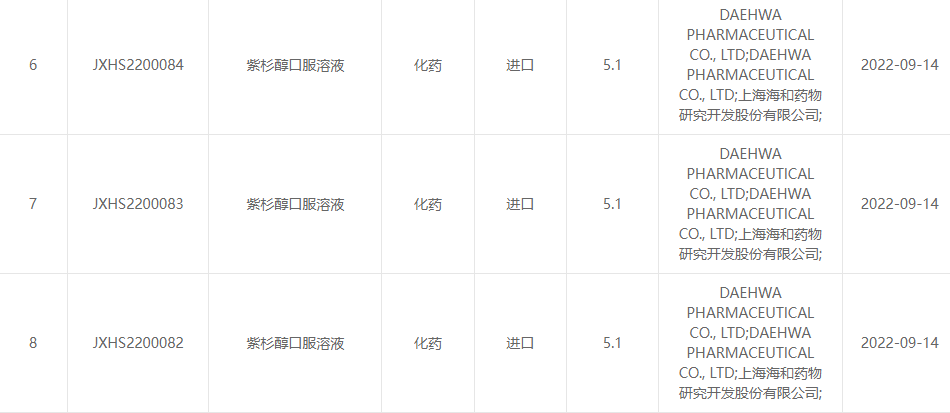
На 13 септември 2022 г. Shanghai Haihe Pharmaceutical Research and Development Co., Ltd. и Daehwa Pharmaceutical Co., Ltd. съвместно обявиха, че пероралният разтвор паклитаксел (RMX3001), разработен съвместно от двете страни, е официално одобрен от Центъра за лекарства Оценка (CDE) на Държавната администрация по лекарствата.(Номер за приемане: JXHS2200082 държава, JXHS2200083 държава, JXHS2200084 държава).
Източник на изображението: Държавна администрация по лекарствата
Паклитакселсе използва широко при лечението на различни злокачествени тумори като рак на белия дроб, рак на гърдата, рак на яйчниците, рак на главата и шията и рак на стомаха.Протеинова полимеризация, сглобяване на микротубули, предотвратяване на деполимеризация, като по този начин стабилизира микротубулите и инхибира митозата на раковите клетки и задейства апоптоза, като по този начин ефективно предотвратява пролиферацията на ракови клетки и играе противораков ефект.
Понастоящем в повечето части на света се използва паклитаксел под формата на инжекция, която трябва да бъде формулирана и приложена чрез интравенозно капково вливане в болницата.Пациентите трябва често да се връщат в болницата и ще има нежелани реакции на мястото на инжектиране.Следователно разработването на перорални препарати с паклитаксел винаги е било гореща точка в индустриалните изследвания..
RMX3001 е перорална формула на паклитаксел, разработена от Dahua Pharmaceutical въз основа на иновативната технология за доставяне на лекарства, самоемулгиращи липиди.Той е одобрен от Корейската администрация по храните и лекарствата през септември 2016 г. (търговско наименование Liporaxel) и показанието е напреднало или втора линия лечение на метастатичен рак на стомаха или локално рецидивиращ рак на стомаха.Според съобщение за пресата от Haihe Pharmaceuticals, Liporaxel е първият перорален продукт с паклитаксел, който е успешно разработен и одобрен за маркетинг в света досега.През септември 2017 г. Haihe Pharmaceutical получи R&D, правата за производство и продажба на продукта в континентален Китай, Хонконг, Тайван и Тайланд от Dahua Pharmaceuticals.
Приложението за вписване на RMX3001 в Китай се основава главно на рандомизирано, отворено, паралелно контролирано, многоцентрово фаза 3 клинично изпитване, което не е по-малка ефективност, което има за цел да сравни лечението от втора линия на паклитаксел перорален разтвор RMX3001 и инжектиране на паклитаксел (Таксол) Ефикасност и безопасност при пациенти с напреднал рак на стомаха.Проучването е проведено съвместно от професор Li Jin от Шанхайската ориенталска болница и професор Qin Shukui от болница Nanjing Jinling като главни изследователи.
Д-р Ruiping Dong, главен изпълнителен директор на Haihe Pharmaceuticals, каза: „Приемането на заявлението за паклитаксел перорален разтвор (RMX3001) е друг важен момент за Haihe Pharmaceuticals и аз съм много благодарен на клиничните изследователи и пациентите, които участваха в нашата пробен период.Рак на стомаха в напреднал стадий Все още има огромна неудовлетворена клинична нужда от лечение и ние се надяваме да предоставим най-модерните иновативни и удобни лечения на пациентите в Китай и по света възможно най-скоро.“
Yunnan Hande Biotechnology Co., Ltd. се фокусира върху производството на паклитаксел от 28 години.Това е първият в света независим производител на растителното противораково лекарство паклитаксел, което е одобрено от FDA на САЩ, европейската EDQM, австралийската TGA, китайската CFDA, Индия, Япония и други национални регулаторни агенции.предприятие.Ако искате да купитеAPI на паклитаксел,моля свържете се с нас онлайн.
Време на публикуване: 14 септември 2022 г